June Sutor y los enlaces de hidrógeno
Uno de los primeros artículos en los que se contaba por primera vez la historia de Rosalind Franklin que, afortunadamente, ya es de dominio público, llevaba la firma de Maureen M. Julian, una cristalógrafa y profesora de la universidad pública americana conocida como Virginia Tech. En su artículo, publicado en 1983 en el Journal of Chemical Education, dentro del apartado Profiles in Chemistry (Perfiles en Química) (ver [1]) criticaba duramente los manejos de James Watson, Francis Crick y Maurice Wilkins para ocultar las contribuciones de Franklin tan decisivas a la hora de desentrañar la estructura de doble hélice del ADN y que les proporcionó a los tres el premio Nobel en 1962.
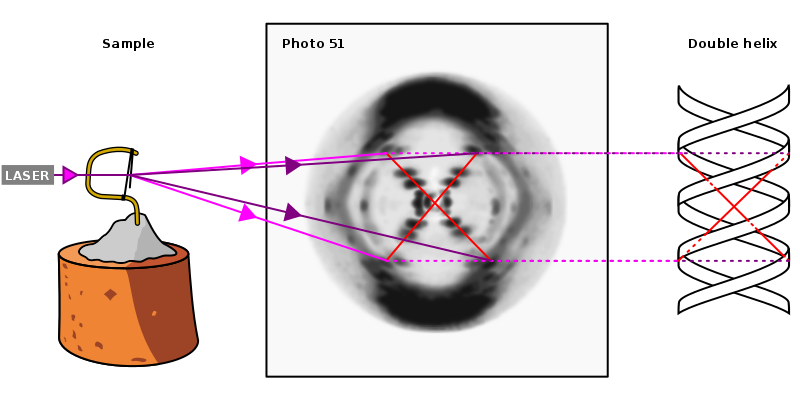
El artículo de la Dra. Julian está trufado de comentarios propios o puestos en boca de otros científicos del campo, como el que hace referencia al ambiente propio de un “club solo para hombres” que imperaba en el King’s College de Cambridge en el que Franklin trabajaba. O lo “atroz” que resulta contemplar ahora el que no se diera crédito alguno a Franklin por su crucial información experimental derivada de sus estudios de difracción de rayos X del ADN. Por solo poner un ejemplo, en las 98 referencias contenidas en las conferencias que los tres ganadores del Nobel impartieron durante las ceremonias de entrega del premio, ni una sola hacía mención a Franklin. Un comportamiento que el artículo denomina “siniestro”, sobre todo si se tiene en cuenta que en el mismo número de Nature donde Watson y Crick publicaron su estructura del ADN (ver [2]), Franklin y Gosling publicaron otro artículo (ver [3]), solo dos páginas después, con su famosa foto 51 y detalles sobre el «timonucleato de sodio», que no es más que la sal sódica del ADN extraído del timo de una oveja.
En la consecución de la estructura de doble hélice del ADN, resulta fundamental el que entre las dos largas cadenas de átomos que la constituyen se establezcan nexos de unión entre partes de una y otra, consiguiendo que, gracias a ello, se doblen de una forma específica. Esas uniones intermoleculares (entre moléculas distintas) se deben en este y otros casos a los llamados enlaces de hidrógeno.
Los enlaces de hidrógeno son también fundamentales en la descripción de algunas propiedades de esa fascinante sustancia que es el agua. El oxígeno de su molécula es más “ávido” por los electrones que comparte con los dos hidrógenos de la misma, lo que hace que soporte una cierta carga negativa mientras que los hidrógeno estén afectados de carga positiva. Como consecuencia de ello, estamos en presencia de una molécula dipolar (dos polos, algo parecido a los imanes) lo que hace que las zonas de distinto signo se alineen o coloquen cercanas, generando clusters o agregados, que son en realidad los causantes (entre otras singulares propiedades) del alto punto de ebullición del agua líquida cuando, por tamaño y la simplicidad de su molécula, tendría que ser un gas a temperatura ambiente.

La autora del perfil de Rosalind Franklin que hemos mencionado al principio, Maureen M. Julian, ha sido una importante fuente de información en un reciente artículo (ver [4]) de Andy Extance, publicado el pasado 8 de julio en Chemistry World. El artículo se centraba en otra mujer ligada al entorno en el que se movió la Franklin, Dorothy June Sutor, también cristalógrafa y experta en difracción de rayos X. Nacida en 1929 en Nueva Zelanda, tras una primera tesis en su país se mudó a Inglaterra, donde realizó una segunda tesis y publicó algunos trabajos sobre la estructura de diferentes purinas, incluida la cafeína. Es en esa primera estancia cuando coincidió con Maureen Julian. Tras un año en el que trabajó en Australia, June Sutor volvió a Inglaterra y, más concretamente, al Birkbeck College de Londres. El mismo College en el que se refugió Franklin durante sus últimos años de vida, lejos del ambiente del King’s College de Cambridge. Allí, junto con John Bernal, hizo importantes contribuciones sobre el uso de la difracción de rayos X en biología molecular.
En 1962, June Sutor publicó un artículo en Nature (ver [5]) en el que explicaba la estructura de ciertas sustancias sobre la base de enlaces entre hidrógenos unidos a un carbono de una molécula y oxígenos de otra. Son los denominados enlaces de hidrógeno tipo C-H….O. Un posterior artículo (ver [6]), en 1963, extendía ese análisis a otras estructuras y detallaba algo más el papel de esos enlaces de hidrógeno. Sus ideas, sin embargo, se encontraron con una formidable oposición, como veremos un poco más tarde.
Al contrario de lo que pasa con los enlaces oxígeno-hidrógeno de una molécula concreta de agua, cuando un hidrógeno está unido por un enlace a un carbono, la tendencia de ambos a “tirar” de los electrones compartidos es muy similar, con lo que la aparición de los excesos o defectos de carga, que veíamos en el caso del agua, es mucho menos evidente, a no ser que otros sustituyentes del mismo carbono tiren de los electrones, como es el caso del cloroformo CHCl3. Pero en esa época no estaba nada claro que en grupos muy habituales, como el grupo metilo -CH3, pudiera darse esa distribución de carga electrónica y el correspondiente carácter dipolar.
Sin embargo, los resultados de rayos X de su artículo de Nature indicaban a Sutor que, en algunas de sus purinas y otras sustancias, las distancias intermoleculares entre hidrógenos de los grupos metilo y oxígenos de otras de sus moléculas, eran menores de lo esperadas. Y Sutor formuló la hipótesis de que esas menores distancias eran debidas a la existencia de enlaces de hidrógeno de tipo C-H….O entre esos grupos.
Jerry Donohue de la Universidad del Sur de California había publicado en 1952 una extensa revisión (ver [7]) sobre el enlace de hidrógeno que, cuando Sutor publicó su artículo en Nature, era tenida como una referencia sobre el tema. Además, Donohue había compartido despacho con Crick en Cambridge y había avisado a éste y a Watson de que sus estructuras para las bases timina y guanina de su ADN estaban equivocadas, lo que afectaba a los enlaces de hidrógeno de la estructura. Ello reforzó aún más su autoridad en el tema de los enlaces de hidrógeno.
Con los artículos de June Sutor ya publicados, el citado Donohue escribió en 1968 un capítulo de un libro (ver [8]) sobre los enlaces propugnados por Suter, en el que desmontaba la mayor parte de sus argumentos, terminando el artículo proclamando, de forma rotunda, que el mencionado enlace de hidrógeno C-H….O propuesto por ella “simplemente no existía”.

Antes de ese demoledor ataque, a Sutor se le habían acabado los fondos para seguir en Londres y en 1963 volvió a su Nueva Zelanda natal. Pero solo tres años más tarde volvió otra vez a Londres, de la mano de la eminente cristalógrafa Kathleen Lonsdale, con quien colaboró prácticamente hasta su muerte en la determinación de la estructura de los cálculos renales (incluida una piedra extraída a Napoleón III) (ver [9]), labor en la que estaba enfrascada cuando Donohue publicó su diatriba contra sus artículos de 1962 y 1963. Pero no consta que Sutor tuviera mucho interés en contestar a esas críticas, que parecieron quedar como bien establecidas entre los cristalógrafos de la época.
Hasta que a principios de los 80, cuando ya estaban disponibles técnicas más potentes como la dispersión de neutrones, Taylor y Kennard (ver [10]) volvieron a estudiar más de un centenar de estructuras similares a las de los artículos de Suter y llegaron a concluir que, para explicar sus estructuras, era necesario echar mano de las distancias más cortas debidas a los enlaces de hidrógeno propugnados por ella.
Cuenta Andy Extance, en su artículo de Chemistry World, que durante la revisión por pares del artículo de Taylor y Kennard, uno de los revisores se permitió ciertos comentarios sarcásticos sobre los orígenes del enlace C-H….O y sobre la propia June Sutor. En casi todas las publicaciones científicas, estas revisiones son anónimas. Sin embargo, parece que, en este caso Danohue, se delató a sí mismo. Extance se atreve a aventurar que el revisor no era otro que el propio Danohue. Quizás no terminaba de asumir su «derrota» a la vista de las de las nuevas pruebas que demostraban las teorías de Sutor. En sus comentarios, denominaba a estos nuevos enlaces de hidrógeno «enlaces Sutor». Nunca sabremos si lo hacía de manera despectiva y con rabia; o bien como una forma poco elegante de atribuir el crédito del descubrimiento a quien realmente lo merecía: la cristalógrafa neozelandesa.
Agradecimiento
Este artículo, en su forma final, contiene varios comentarios y correcciones de ese excelente comunicador científico que es Fernando Gomollón Bel.
Referencias
[1] M.M. Julian, Rosalind Franklin: From Coal to DNA to Plant Viruses, J. Chem. Educ. 60 (1983) 660-662
[2] J.D. Watson and H.F. Crick, Molecular structure of nucleic acids; a structure for deoxyribose nucleic acid, Nature 171 (1953) 737-738
[3] R.E. Franklin and R.G. Gosling, Molecular Configuration in Sodium Thymonucleate, Nature 171 (1953) 740-741
[4] A. Extance, The forgotten female crystallographer who discovered C–H⋯O bonds, Chemistry World, 8 julio 2019
[5] D.J. Sutor, The C–H… O Hydrogen Bond in Crystals, Nature 195 (1962) 68-69
[6] D.J. Sutor, Evidence for the existence of C–H⋯O hydrogen bonds in crystals, J. Chem. Soc. (1963) 1105-1110
[7] J. Donohue, The Hydrogen Bond in Organic Crystals, J. Phys. Chem. 56 (1952) 502-510
[8] J. Donohue, Selected Topics in Hydrogen Bonding. En Structural Chemistry and Molecular Biology: A. Rich and N. Davidson, Eds.; Freeman: San Francisco, CA, 1968; pp. 443-465
[9] D.J. Sutor, Newberyite—its Formation in Human Urinary Calculi, Nature 218 (1968) 295
[10] R. Taylor and O. Kennard, Crystallographic evidence for the existence of C-H….O, C-H….N and C-H….Cl hydrogen bonds, J. Am. Chem. Soc. 104 (1982) 5063-5070
Sobre el autor
Juan J. Iruin es Catedrático (retirado) de Química Física en la Facultad de Química de la UPV/EHU en San Sebastián. Desde 2006 mantiene el Blog del Búho, sobre diversos aspectos de la Química en nuestra vida cotidiana.
3 comentarios
Ya lo había escrito Isaac Newton. «Sólo andamos sobre hombros de gigantes»»
Qué bien por los científicos, mujeres y hombres.
Saludos.
Es muy importante reconocer mujeres importantes para la historia. Muchas gracias!
Hola Caba, por supuesto que tienes mucha razón, no solo es importante conocer a las científicas, sino que la historia de la ciencia no puede considerarse completa sin tener en cuenta las aportaciones de las mujeres: han sido muchas, algunas brillantes, otras simplemente buenas, pero todas imprescindibles. Un cordial saludo