
Imagínate la siguiente situación: un día te despiertas y tus familiares te preguntan a ver qué te pasa. Tú no sabes sobre que te hablan y ellos te dicen que tu actitud mental ha cambiado. No le das importancia. Después, te empiezas a desinteresar por el trabajo que antes te encantaba, y empiezas a sentarte y a descansar más a menudo de lo habitual. ¿Será un periodo de simple vagancia? Pero empiezas a tener dolores de cabeza y otros dolores transitorios, como ese dolor de pecho que tanto te molesta. Te miras en el espejo y algo ha cambiado en tu rostro. Antes te mirabas y veías una cara de felicidad con un toque de inteligencia, pero ahora más bien tienes un rostro apático y sin brillo. Pasan los días, y empiezas a tener fiebre a las noches, sin embargo, a la mañana la temperatura está más baja de lo normal, y tu pulso varía de 90 a 130 latidos por minuto. La somnolencia que ha ido en aumento cada día, ahora se convierte en un coma, y un día mueres sin que te des cuenta porque estas sumergido en un profundo sueño.
Parece una película de terror, ¿verdad? Pues ésta era la realidad que sufrían cada día en África durante varias décadas de los siglos XIX y XX. Se trata de la enfermedad del sueño o tripanosomiasis africana, una enfermedad bastante conocida mundialmente, al menos por el nombre coloquial. Eso sí, lo que el mundo no conoce es el nombre de la científica a la que debemos el tratamiento de la enfermedad: Pues bien, se trata de Louise Pearce.
Nacida en Winchester, Massachusetts, Louise Pearce (1885-1958) era la hija mayor de Susan Elizabeth Hoyt y Charles Ellis Pearce, que se mudaron junto con el hermano Robert a California. Allí, Pearce asistió al colegio “Girls Collegiate School” en Los Ángeles. En 1907, Louise obtuvo el grado A.B. en fisiología e histología en la Universidad de Stanford. Fue miembro de una Fraternidad de Mujeres llamada Pi Beta Phi (ΠΒΦ), que fue la primera fraternidad nacional secreta de mujeres basada en la fraternidad masculina “letra-Griega”. Desde 1907 hasta 1909 estuvo en la Universidad de Boston, y fue admitida en la Escuela de Medicina de la Universidad Johns Hopkins (JHUSOM). Después de obtener el doctorado en medicina por el Johns Hopkins, siendo la tercera de su clase en graduarse, trabajó durante un año en el hospital como residente, sirviendo en la clínica Phipps Psychiatric Clinic. A pesar de que su carrera no había hecho más que empezar, ya parecía que iba a ser una excelente científica, ya que el Dr. Welch del Johns Hopkins la recomendó como “una prometedora médica patóloga”.
Un año después de obtener el doctorado en medicina, en 1913, Pearce consiguió una posición de investigadora en el Instituto Rockefeller, siendo la primera mujer a la que se le designaba ese título. La patóloga permanecería allí para el resto de su carrera, esto es, desde 1913 hasta 1951. Durante sus primeros años en el Instituto, trabajó para el director, el Dr. Simon Flexner. Viendo que era excelente en su trabajo, en 1923 la ascendieron a miembro asociado, y durante mucho tiempo trabajó junto con el patólogo Dr. Wade Hampton Brown. Sin embargo, a pesar de ser brillante como científica, nunca llegó a ser miembro de pleno derecho del instituto, lo que una vez más nos hace pensar que fue discriminada como científica por ser mujer.
¿Sabías que… las moscas tse-tsé no crean la enfermedad del sueño?
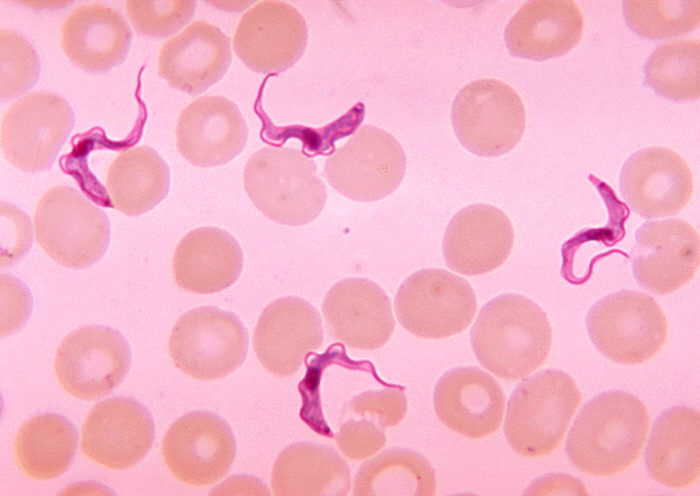
Así es. Aunque mucha gente relacione estas moscas con la enfermedad en sí, en realidad solo transmiten el parásito que crea la enfermedad. Por lo tanto, las moscas tse-tsé no crean la enfermedad. Los tripanosomas, esos son los parásitos unicelulares culpables de la enfermedad, y a pesar de que existan varios tipos, el causante más habitual de la tripanosomiasis africana (enfermedad del sueño) es el Tripanosoma brucei. Hablemos un poco de éste.
Una característica muy importante de Tripanosoma brucei es que puede cambiar su forma celular dependiendo del ambiente que lo rodea. Se presenta de dos diferentes formas y depende del flagelo de la célula o “la cola” de la célula (dicho de una manera muy coloquial). La primera forma se llama Epimastigote, que significa que el flagelo está conectado al cuerpo de la célula por una membrana ondulada corta. La segunda, en cambio, se llama Tripomastigote, y está conectada por una membrana ondulada larga. Además, para explicar el ciclo de vida de este parásito, es importante saber que dentro de la forma tripomastigote existen cuatro subtipos: procíclico (presente en el intestino de la mosca y proliferativo o capaz de reproducirse), metacíclico (presente en las glándulas salivares de la mosca y no reproductivo), esbelto (presente en el flujo sanguíneo del humano y proliferativo) y corto (presente en el flujo sanguíneo del humano y no proliferativo). Y pensaréis, “Pero… ¿por qué presenta tantas formas?”. La respuesta es que al pasar por diferentes ambientes (como por ejemplo, el flujo sanguíneo humano y el intestino de la mosca, entre otros) se adapta para sobrevivir en cada uno de ellos.
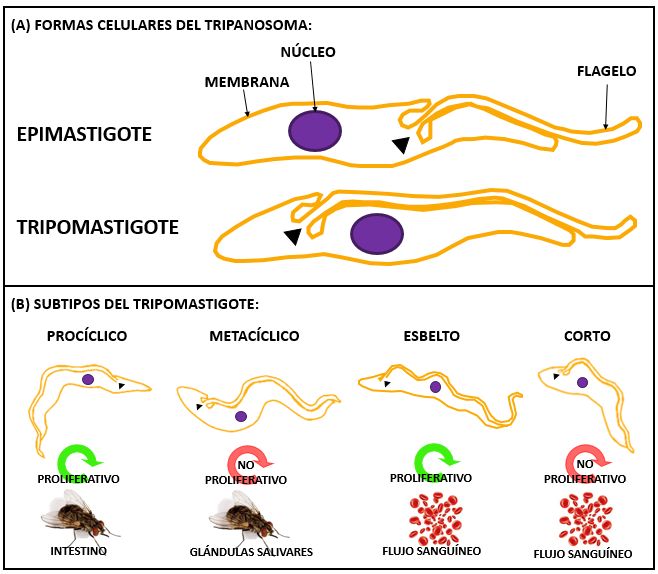
esto es, su inicio. Creado por Arantza Muguruza Montero.
Una vez que se han aclarado estos conceptos, empecemos a explicar el ciclo: cuando una mosca tse-tsé pica a un humano para alimentarse de su sangre, una parte de su saliva entra en su cuerpo, por lo que, si la mosca está infectada con este parásito, inyectará en el humano tripanosomas metacíclicos. Una vez que el parásito está en el flujo sanguíneo del humano se convierten en tripomastigotes sanguíneos esbeltos, esto es, empiezan a reproducirse ya que las condiciones en las que se encuentra son favorables. Además, en esta forma es capaz de hacer frente a la respuesta inmune del humano y esto hace que la infección se expanda creándole síntomas al huésped. Teniendo en cuenta que los parásitos se aprovechan del anfitrión para alimentarse, una vez que se han reproducido mucho, esto es, cuando hay demasiados parásitos en la sangre del humano, reciben señales para que cambien a la forma tripomastigotes cortos. Éstos, no son capaces de reproducirse. Es como si ellos mismos dijeran: “Vamos a dejar de reproducirnos porque si no, no vamos a caber aquí…”. Además, este subtipo es una preadaptación a la mosca tse-tsé, o sea que se están preparando para “mudarse” a la mosca. Los tripomastigotes cortos esperan en la sangre del humano hasta que una mosca pica al humano. Entonces, junto con la sangre, los tripomastigotes cortos pasan al intestino de la mosca. Y allí, se transforman en tripomastigotes procíclicos y se multiplican. Algunos de esos, pasarán a las glándulas salivares de la mosca. Por las condiciones de estas glándulas se transformarán en epimastigotes y empezarán a reproducirse. Finalmente, se transformarán en tripomastigotes metacíclicos, que no son capaces de reproducirse, por la misma razón de antes.
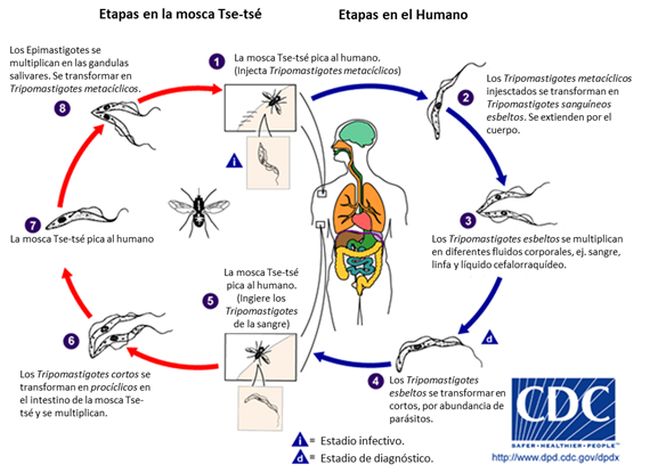
Es importante mencionar también, que la enfermedad se separa en dos fases. En la primera los tripanosomas se multiplican en la sangre y en la linfa causando episodios de fiebre, dolores de cabeza y de las articulaciones, y picor de piel. En la segunda fase, los parásitos cruzan la barrera sanguínea del cerebro e infectan el sistema nervioso central. En esta fase los síntomas son más evidentes, pues causan cambios de comportamiento, confusión, alteraciones sensoriales y del ciclo de sueño.
La investigación principal de Pearce
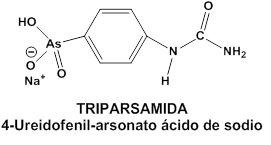
Como ya he mencionado antes, la enfermedad del sueño era una epidemia devastadora que despobló distritos enteros en África. Hoy en día, se conoce tanto la transmisión como el mecanismo de la enfermedad, pero hasta 1903 no se sabía absolutamente nada acerca de la enfermedad del sueño. En esa época se propusieron algunas preparaciones que contenían arsénico como tratamiento para la tripanosomiasis, pero ninguno de ellos era eficaz. Simon Flexner organizó un grupo en el Instituto Rockefeller con el fin de testar diferentes compuestos arsénicos. Teniendo en cuenta el trabajo del alemán Paul Ehrlich, que desarrollo un fármaco derivado del arsénico llamado Salvarsan para el tratamiento de la sífilis, el químico Walter A. Jacobs y el inmunólogo Michael Heidelberger sintetizaron 243 posibles componentes arsénicos, variando algunos grupos químicos (como los grupos metilos, amidas y las cadenas laterales complejas). El objetivo de Pearce y de su colega Brown era estudiar los diferentes modelos animales de la enfermedad, esto es, testaron los posibles tratamientos en ratas, ratones y conejos, con el fin de comprender mejor el curso de la enfermedad y de probar la efectividad inicial de los componentes. Un trabajo laborioso teniendo en cuenta que había que probar los 243 posibles componentes en tres modelos de animales diferentes. Se dieron cuenta de que en las ratas y los ratones, los parásitos tendían a permanecer en el corriente sanguíneo, mientras que en los conejos invadían el sistema nervioso central, este último un modelo más comparable al ser humano.

Después de tanto trabajo, el fármaco que más posibilidades de éxito tenía era la triparsamida; en 1912 se publicaron los resultados exitosos en el Journal of Experimental Medicine. Por ello, en 1920, el Instituto Rockefeller envió a Louise Pearce a Léopoldville, a la actual República Democrática del Congo, para testar la triparsamida. Allí, trabajó en el laboratorio de un hospital local, para diseñar y llevar a cabo un protocolo de testado del fármaco en ensayos clínicos con humanos. Así se podría establecer la seguridad de la triparsamida, su efectividad y la dosis óptima. ¡El tratamiento fue un éxito! La mayoría de los pacientes, incluso en aquellos que se encontraban en estadios tardíos de la enfermedad, se pudieron salvar. Sin embargo, los ensayos clínicos también relevaron que a altas concentraciones o repetidas dosis, la triparsamida podría crear un efecto secundario: el daño al nervio óptico y la consecuente pérdida de visión. No obstante, la triparsamida se convirtió en la “droga de moda” para la quimioterapia en la enfermedad del sueño durante décadas, porque era fácil de administrar, actuaba rápido y curaba más del 80% de los pacientes. Siendo un compuesto capaz de entrar en el sistema nervioso central, era el primer fármaco que se podía usar para tratar los estadios tardíos de la tripanosomiasis africana.
Por lo tanto, Pearce no solo hizo un grandísimo trabajo al probar tantos diferentes posibles tratamientos para la enfermedad del sueño, si no que determinó cual podría ser el tratamiento adecuado y lo demostró en pacientes humanos.
De la enfermedad del sueño… a otras investigaciones
Además de la tripanosomiasis africana, Pearce y Brown estudiaron la sífilis en conejos durante un periodo de seis años. Llegaron a entender la enfermedad y se dieron cuenta que seguía un curso parecido en conejos y en humanos. Aprovechando el tratamiento que ya habían investigado, usaron la triparsamida contra la sífilis. Y a pesar de que funcionaba mejor contra los tripanosomas que con las espiroquetas, las bacterias causantes de la sífilis, era un tratamiento útil por su habilidad de pasar la barrera hematoencefálica o barrera sangre-cerebro. Gracias a estos dos investigadores, se usó la triparsamida como tratamiento contra la sífilis, hasta que en 1950 fue reemplazada por la penicilina.
Enfermedad del sueño, sífilis, el uso de la triparmasida contra las dos enfermedades… Fueron investigaciones intensas y largas, pero no fue lo único. Durante una de sus investigaciones con conejos, descubrieron un tumor maligno del epitelio del escroto, y hoy en día se conoce como el carcinoma de Brown-Pearce, que es famoso por ser un tumor trasplantable. Llegaron a entender su transmisión, su crecimiento y su remisión, y gracias a sus profundas investigaciones y a que los experimentos eran completamente replicables, esto es, que se repiten siempre que se hacen, el tumor de Brown-Pearce se usó mucho en otros laboratorios de investigación del cáncer.
Después de que Brown muriera en 1942, Pearce continuó investigando y recolectó una gran cantidad de datos con información sobre senescencia temprana o envejecimiento humano temprano, acondroplasia (causa común del enanismo), osteopetrosis (enfermedad que se caracteriza por tener los huesos muy densos), defectos oculares, enfermedad quística e hidrocefalia (enfermedad que se caracteriza por tener demasiado líquido cefalorraquídeo en el cerebro).
No todo era el laboratorio
Si algo está claro es que esta mujer fue una gran investigadora, con una carrera muy fructífera, y gracias a su trabajo fue miembro de varias asociaciones. Por poner algunos ejemplos, en 1915 la eligieron como la primera miembro femenino de la Sociedad Americana para la Farmacología y Terapéutica Experimental (ASPET); en 1945 fue directora de la Asociación de Mujeres Universitarias Americana (AAUW); y desde el año 1946 hasta el 1951 fue presidenta del Colegio Médico de Mujeres de Pensilvania.
A pesar de que se desconoce la fecha exacta (1920 o 1921), Pearce recibió la Orden de la Corona de Bélgica (Order of the Crown of Belgium) que es uno de los premios más honorables de este país. Además, en 1953, el rey Leopoldo II la premió con 10 000 dólares y la Royal Order of the Lion. Y como en la ciencia nunca se trabaja en solitario, sus colegas también fueron honrados por sus contribuciones.
Pero no solo era una gran trabajadora e investigadora. Louise Pearce era miembro de Heterodoxy, un grupo de debate feminista, en el cual muchas de sus miembros eran lesbianas o bisexuales. Éste es un detalle que merece la pena mencionar, ya que, en esa época, la sexualidad estaba muchísimo más marcada por la sociedad, y el rol de la mujer era “casarse con un buen marido” para que “le diera unos buenos hijos” y “cumplir bien con las tareas del hogar”. Pearce rompió por completo las “reglas de la sociedad” de entonces. Para empezar, se hizo un hueco en el difícil universo de la investigación. Pero es que además, vivió con la física Sara Josephine Baker y la autora Ida A. R. Wylie, que también pertenecían al grupo Heterodoxy, y su casa se describía como “el lugar más encantador e interesante para vivir y estudiar”. Después de que Baker falleciera en 1945, Wylie y Pearce siguieron viviendo juntas hasta 1959, año en el que ambas murieron.

Bibliografía
- Louise Pearce, Wikipedia
- Dr. Louise Pearce, Changing the Face of Medicine
- Louise Pearce (1885-1959), Smithsonian Institution
- Trypanosoma brucei, Wikipedia
- La tripanosomiasis africana (enfermedad del sueño), Organización Mundial de la Salud, enero 2017
Sobre la autora
Arantza Muguruza Montero es graduada en Biotecnología por la UPV/EHU, estudiante del máster en Biología Molecular y Biomedicina de la UPV/EHU y alumna interna en un grupo de investigación del Instituto Biofisika.